通常,一款新疫苗从开始研发到成功上市,短则三五年,长则十几年。世界卫生组织推测,新冠病毒疫苗问世需要12~18个月。为何它会比一般疫苗快?又为何不能更快些?这或许是同一个问题。
冠状病毒疫苗 | https://www.genengnews.com
作者 | 徐斯佳 日本京都大学医学院
编辑 | 龙浩
疫苗是人类战胜重大传染病的终极解药。目前全球新冠病毒感染人数已累计超过400万,新确诊病例数以每日约8万人的速度持续增加中。
前期宣传较好的几种新冠“特效药”最近陆续传出负面消息,人们对疫苗成功研制的期盼与日俱增。
截至目前,全球共有8款新冠疫苗进入了人体临床试验,其中4款来自中国。
世界卫生组织推测新冠病毒疫苗问世需要12~18个月。这比一般疫苗的开发周期短很多。为什么它能比其他疫苗更快?又为何不能更快一些?
理解这个问题,需要我们看到疫苗研发的多面:比如,已有的基础,不能跨越的规律。我们试图全面梳理一下。
疫苗之难:服务庞大人群,注定万里挑一
药物研发的成败总取决于两个关键:有效及安全。
疫苗是一类非常特殊的药物。它保护的是健康人群,数量较之患者可多出千万倍,因此合格的疫苗必须满足更为严格的疗效和安全性要求。
简单举例,假设有2种疫苗,发生严重不良反应的概率分别为0.1%和0.2%,乍一看数值都很低,但给1亿人使用,影响人数就可能有10万人之差,显然谁都不想成为其中之一。
所以,能被大规模使用的疫苗都是经历重重考验、万里挑一的尖子。过去50年,有44种危害人类健康的病原体被发现,但只有6个疫苗成功上市。
病毒疫苗的研发大致有5个必经阶段:毒株分离测序→候选疫苗制备→动物模型验证→人体临床试验→量产投入使用。
通常,一款疫苗从研发到成功上市,短则三五年,长则十几年。对于新冠疫苗,世卫组织的推测是12~18个月,比正常周期短很多。
对于这个估计,有些人会想:这是否是以牺牲安全性为代价?另一些人则可能不解:眼下全世界的政策和资金都在支持研发,各种顶尖机构参与,为何还要等到明年?
两个疑问都有道理。
要回答这两个截然相反的问题,还是得从疫苗的研发流程说起。
STEP1 毒株分离测序:“中国速度”创造历史
俗话说,巧妇难为无米之炊。疫苗研制的第一步,是从患者样本中分离出毒株,并获得其全基因组序列。这是设计候选疫苗的原材料和必要参考。
得益于飞速发展的分离和测序技术,中国科学家迅速响应,这一步以史无前例的速度完成了:首个感染病例被确诊后仅1个月,1月11日,中国科学家便鉴定出病毒种类,并向世卫组织共享了其全基因组序列。——当年的SARS病毒,可是耗时了4个多月才获得。
仅半个月之后,1月28日,国内外多家机构陆续分离出新冠病毒毒株,病毒的“个人档案”被人类掌握,各类候选疫苗的筛选陆续启动。

病毒的全基因组序列是新疫苗研制的必要参考| hstoday.us
STEP2 制备技术大比拼:传统方法更值得期待
有了原材料,下一步是选择合适技术进行疫苗的筛选和制备。
疫苗的原理,是模拟病原体特征,让人体免疫系统提前来一场军事演习,产生战斗记忆和抗体,这样在未来病毒来袭时就能轻松应对。所以无论技术新旧,都是变着法子引导人体认出病原体,保证演习有效且安全地展开。
怎样才能达到这个目的呢?关键是对病毒特征的模拟。疫苗制备技术的进步,可以说是来自人类对病毒拆解能力的不断提升。
起初人们连分离毒株都很费劲,为了预防天花,还曾拿病人皮疹上的脓液或结痂直接往健康人身上涂。
后来逐渐学会分离病毒,就开始对其进行加工,比如将其整体灭活,或减弱毒性,或仅提取其“零部件”,给免疫系统做演习之用。通过这些方法生产的疫苗,被归为传统疫苗。(分别对应:灭活疫苗、减毒活疫苗、亚单位疫苗)
后来出现的依托基因工程技术生产的核酸疫苗和载体疫苗,则不需要病毒真身参与,而是通过人工合成,就像复印了病毒的“身份证”,送入人体做备案,它们可以归为新技术疫苗。
目前我国已有4个疫苗进入临床试验,包括3个灭活疫苗和1个腺病毒载体疫苗,技术流程都比较成熟。而国外的几个在试验疫苗则为核酸疫苗。
· 几种常见疫苗 ·
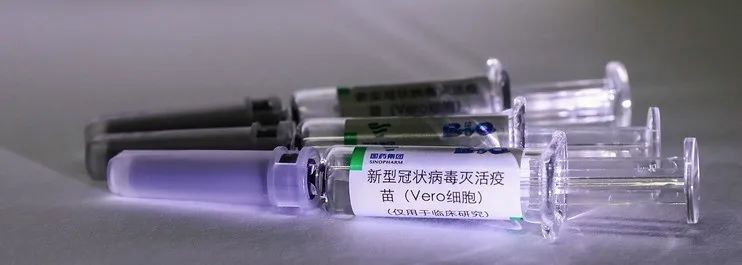
灭活疫苗,也称死疫苗,是历史悠久的传统疫苗之一。原材料是病毒本身,通过物理或化学方法将病毒的蛋白质凝固,去除其感染活性,但保留能被人体免疫系统识别的“外貌”特征。好比将凶狠的野兽制作成不会动弹的标本。其稳定性和安全性比较可靠。但死疫苗在人体内不能繁殖,对免疫系统的刺激时间短,需多次接种才能达到理想效果。(图| 我国已进入临床试验的灭活疫苗之一,新华社)
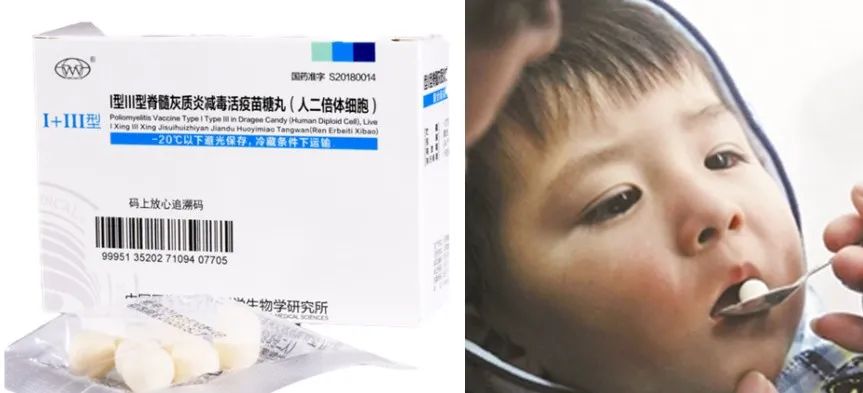
减毒疫苗可以弥补灭活疫苗的不足,它是保留了病毒复制能力的活疫苗,也是传统疫苗研制的热点。通过改变病毒的生存环境,例如,将病毒感染其他宿主细胞、或养在低温环境中,再反复传代,适应了新环境的病毒对人体的毒性便逐代减弱。被减毒的病毒是活的,接种后能在体内温和繁殖,激发较持久的免疫反应。接种次数少,副反应轻微。我们所熟悉的麻疹疫苗、冻干水痘疫苗,还有小时候吃的“糖丸”脊髓灰质炎疫苗,都属于减毒活疫苗。它好处虽多,但毕竟是活疫苗,毒性有可能反强,对老人儿童等免疫力较弱人群的安全性要仔细考量,筛选会更费时,因此这次率先进入临床试验的还是灭活疫苗。(图| 小时候吃的“糖丸”疫苗,来自网络)
腺病毒载体疫苗,也是一种活疫苗,和减毒活疫苗颇有异曲同工之妙。疫苗中使用的是经过人工改良的腺病毒,温和不致病,但仍有自我复制能力。我们知道,新冠病毒是靠表面的特殊的棘突S蛋白入侵人体细胞的。腺病毒载体疫苗就是先将新冠病毒编码S蛋白的基因插入改良腺病毒的基因组中,然后像一辆辆载货的卡车,被注射入人体。随后它们每次复制,都会顺带把插入的新冠病毒S蛋白基因一起复制、编码,给人体免疫系统练兵,产生针对的抗体。我国军事科学院陈薇院士团队研制的腺病毒载体疫苗是全球首个进入二期临床试验的新冠疫苗,值得期待。
核酸疫苗,是国外机构重点研发的疫苗,它不借助载体,直接将编码病毒蛋白的核酸片段导入人体细胞,利用人体自己的细胞工厂,合成出蛋白,诱导免疫应答。核酸疫苗的好处是成分简单,可以大量人工合成;缺点是核酸不稳定,而且要依赖其他细胞环境把上游核酸变成下游蛋白,中间各个步骤可能受到诸多因素影响,不一定能成功引起免疫应答。历史上尚无核酸疫苗成功上市。多一种技术当然多一份希望。
不同种类疫苗各有优缺点,但无论用何种技术, “有效”和“安全”都是判断疫苗成败优劣的唯二标准。
就目前来看,传统疫苗的制备工艺简单,技术路线成熟,竞争力并不比新技术疫苗差,甚至更值得期待。
STEP3 动物模型有基础,“库存”小鼠直接用
试验疫苗制备完成之后,就要开始筛选了。动物模型(即代替人类做“人体”试验的动物)是筛选疫苗的重要工具。
对于一种新发疫情,找到感染症状和人类相似的动物通常很困难。好在新冠病毒和2003年的SARS病毒有很大相似性。它们都属于冠状病毒家族,都通过棘突蛋白S与人细胞表面的血管紧张素转换酶2(ACE2)蛋白结合,继而入侵人体细胞。
而当年研究SARS病毒时发现,科研中最常用的试验动物——小鼠,由于物种特异性,不能自然感染SARS病毒。所以一开始只能用昂贵的猴子,在国内极少数特殊实验室中进行研究。
直到后来,用基因编辑技术构建出了表达人类ACE2蛋白的小鼠,并筛选出能模拟出类似的肺部病变的感染条件,这才大幅改善了SARS病毒研究的成本和效率。
此次新冠疫情初期,尚没有专一动物模型之际,科学家们在确认了新冠病毒与SARS病毒的亲缘性后,先借用SARS病毒易感小鼠来开展疫苗的动物验证,再次加快了候选疫苗的研发进程。
动物模型是筛选疫苗的重要工具| medicilon.com.cn
STEP4 人体(临床)试验I-III期,不只是人数的递增
候选疫苗通过动物实验之后,就要进入“实战”了。
疫苗的人体试验通常分三期进行。规模上至少需要数十人、数百人和千人级别。但其实每一期的意义和任务都不同,绝不只是人数上的差异。
首先,对一种初次在人体上测试的新药来说,安全与否比确认效果更重要。因此小规模的I期临床试验,主要任务就是判断疫苗的人体安全性和可耐受剂量。通过给与梯度剂量(从少到多)的疫苗,观察不良反应和剂量的关系,并收集药物在体内的代谢信息,如吸收效率,有效浓度,代谢产物和排泄途径等。
II期临床试验承上启下。这个阶段会设置对照组。除了进一步确认不良反应在数百人规模中的发生率,将重点考察疫苗的保护效果、确认发挥最佳效果的疫苗剂型等,为III期试验的设计和给药剂量等提供依据。
而III期临床试验是疫苗是否能上市的决定性阶段,也是法律规定的必经环节。I、II期临床试验最短各需要1个月完成,而III期临床试验最短需要3~5个月完成。当然,这是最顺利的情况,实际上,由于各种未知与意外,III期临床试验持续数年的情况十分常见。
理想的III期试验应是在国内外多处医疗中心开展双盲、对照试验,因为不同地域人群的基因差异、各机构的检验效应等都可能影响疫苗的效果。III期试验的方案设计和实施要求最严格,难度也最高,历史上许多项目都是在III期试验阶段功亏一篑。
目前尚无新冠疫苗进入III期试验。陈薇院士团队的腺病毒载体重组疫苗第II期试验的508个志愿者已经注射完毕,预计本月揭盲。

III期临床试验涉及极其复杂的科学设计| kknews.cc
STEP5 走向量产:技术政策齐加速,历史教训引深思
新冠疫苗的研发之所以能达到空前速度,有各种因素的助力:
技术进步让我们能更快分离出原始毒株,确定其基因组序列;依靠基因组序列,我们又迅速确认了新冠病毒与SARS病毒的家族相关性,并借用SARS病毒的动物模型,快速启动候选疫苗的制备和动物试验。
由于疫情逼迫,各国政府和组织均对疫苗研发给予了最大程度的支持,包括资金倾斜、简化审批手续。比如,我国授予部分项目I期和II期合并临床试验的许可,理论上可至少缩短1个月的进程。这些都是迄今为止疫苗研发能达到的最快加速。
即使如此,我们却可能再次面临当年SARS疫苗研发后期遇到的窘境:
随着中国新确诊病例趋零,适合疫苗III期临床试验的本土环境将逐渐消失。如果病毒暴露条件不足,就无法判断感染者数量的减少是否是疫苗起了作用。
如果III期研究只在国外疫情流行地区开展,病毒暴露环境将是真实的,保护效果也易于观察,但得到的数据并不能代表中国人群病毒暴露下的疫苗效力,得到的结论是否能被用于中国人群,也是一个疑问。
有专家提出过替代方案,比如将归国、出国人员等作为试验对象,或启动“应急接种”,对海关、机场等特定场所的一线抗疫人员注射疫苗。这样,病毒暴露环境就接近真实。
但依然存在样本人数偏少、无法覆盖全年龄层、归国人员的隔离措施必须被迫放宽等问题。
如果这些问题无法得到合理解决,无疑将影响到III期试验的耗时和结果的准确性。

确诊人数趋零,可能导致无法开展III期临床试验 | 来自网络
另外,由于疫苗研发的周期非常长,经常出现这样的尴尬局面:病毒一来,各种研究项目一哄而上、万众瞩目;病毒消停,则一哄而散,很多项目中途撤项、不了了之,造成巨大的资源浪费。
如果新冠病毒最终成为像流感那样的季节性流行病毒,那疫苗无疑将是最重要的防治措施。但即使没有,从SARS、MERS到此次的新冠病毒也可以看出,冠状病毒家族俨然已成为人类的“老朋友”,鉴于病毒结构的一脉相承,难保何时又有哪位家族成员一时兴起,窜出来帮我们梳理人生。
因此有专家倡议,应充分考量各个机构设计疫苗和实现技术转化的能力,集中资源继续支持个别有希望出成果的项目,即使疫情消退也给予持续的支持,并重视广谱冠状病毒疫苗的研发,为未知的危险做准备。
平静安宁的日子是我们每个人的美好愿景,但确实不应再心存侥幸。面对新的天灾,疫苗总是姗姗来迟。经此一役,各国想必已达成共识:无论眼前还是往后,我们只能始终带着严谨而敬畏的心态,做好与无常疫病长期作斗争的准备。
参考资料:
1、http://m.xinhuanet.com/2020-04/17/c_1125869116.htm
2、http://dl.gov.cn/yqfk2020/info/1049262_1071339.vm
3、赵恺.疫苗研究与应用[M].人民卫生出版社, 2013
