8月5日,《科学·进展》期刊发表我国学者论文,其上登载了一张“药物击靶”显微镜照片。照片显示:当药物分子(硫黄素T)要与生命体内的靶蛋白结合、起药效时,不是像人们想象的单个分子去结合蛋白,而是自动像“乐高积木”一样组装后,合力“击靶”,这种“机灵劲儿”与之前人们的想象完全不同。
本以为它只身赴命,没想到它两两成对、凑四成团、甚至6人成伍……
这个新发现可能带来哪些颠覆性改变?为什么之前没拍到过这样的照片?药物分子又靠什么像“乐高”一样自动组装?带着这些问题,8月12日,科技日报记者专访了论文通讯作者之一的中国医学科学院基础医学研究所副研究员王晨轩。
首张显微镜照片究竟能看到什么?
俗话说:外行看热闹,内行看门道。
一张照片能传递哪些信息?全靠怎么看。
“教科书中有一个经典的‘锁钥模型’,是说药物分子能够‘击靶’必须要和蛋白严丝合缝,像一把钥匙开一把锁,但现在的显微镜观测结果表明,药物分子用寡聚态的方式‘工作’,或许我们只需要半个钥匙就能开锁。”王晨轩对科技日报介绍,这是科学家首次直观看到“药物击靶”的状态,可用于指导药物分子的设计。
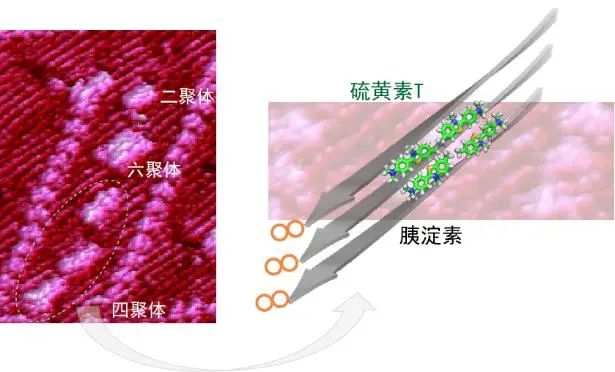
研究团队发现药物(硫黄素T)在受体蛋白表面上的结合结构以寡聚态存在
先说这张照片的主角。它们是药物分子硫黄素T,和它的靶点分子——胰淀素蛋白(淀粉样蛋白的一种)。
为什么选择这两个主角做研究?王晨轩说,作为生命大分子,蛋白质一旦出错经常会“缠绕”错乱,从正确的折叠构象向错误的折叠构象转变,最后形成淀粉样的沉淀,因此淀粉样蛋白和很多疾病相关。
人们最耳熟能详的淀粉样蛋白是β-淀粉样蛋白,它被发现在老年痴呆症患者的神经细胞中频繁出现,很多药企花巨资想研究怎么让这些淀粉样沉淀消失,至今都没有成功。
还有二型糖尿病、亨廷顿舞蹈症等等,这些疾病中都有淀粉样蛋白的身影。因此研究它们与药物分子的作用机理对很多疾病有帮助。
硫黄素T正是能和这些“病态”淀粉样蛋白特异性结合的分子,而且它还有显色的优势。
这对照片上的主角,实际上背后关联的是很多现在没有解决办法的疾病。
照片中的主角干啥了?
硫黄素T两两成对、凑四成团、甚至6人成伍。用学术的说法是:研究团队发现硫黄素T在受体蛋白表面上的结合结构以四种寡聚态存在,即二聚体(头尾相接)、二聚体(肩并肩相接)、四聚体、六聚体。
看到这样一幕为啥要激动?这就是药物分子能像“乐高”积木自动组装拼接的最好证据!
没看到之前,人们要么认为药物分子只能“单着”,要么靠“盲算”揣测它们的结合,但是压根没证据,也就更无法指导实践了。而之后,药物设计者,可以大胆地将选择性寡聚效应应用于药物分子的结构设计与优化中,通过理解药物的寡聚化机理并操纵寡聚结构,以药物团簇而不是药物单分子为“单元”靶向受体蛋白。
显微镜照怎么拍出来的?
面对首张“药物击靶”显微镜照,很多人会问:为什么以前拍不出来?
答:设备和方法达不到要求。
蛋白质的照片拍摄困难,先是晶体衍射法,再是冷冻电镜的方法,但是至今仍不是所有的蛋白都能拍摄成功。原因是都必须要让蛋白排列成有序的阵列,才能满足成像要求。
“这就好比,只有阅兵式上的解放军方阵才能成像,而后面的群众大联欢方阵是拍不上的。”王晨轩打了个特别形象的比方,因此要拍摄和药物分子结合的蛋白分子,就要用新的拍摄设备。
扫描隧道显微镜勇担重任。“它最初是物理学家用来探测原子、亚原子的微观结构,具有超高的分辨能力。”王晨轩说,把物理设备引进生物领域是上世纪90年代的事情,需要完成对设备的硬件、软件、算法的全新研制,中国团队在国际上是较早进入这一领域的。

由于它是利用量子力学中的隧穿效应,通过记录穿越样品的电子直接捕捉蛋白质和药物分子的“模样”。最开始的扫描隧道显微镜操作必须在真空中。
中国科学家团队很早解决了常态下用扫描隧道显微镜观测的问题,在世界上首次使用了扫描隧道显微镜,实现了在大气室温下对化学分子的观察。
“国内学者经过几代人的不断传承,持续改造设备、开发新的数据采集方法,我们才充分展示它的能力。”王晨轩说。
为了拍摄首张“药物击靶”显微镜照,医科院基础所王晨轩、于兰兰、张文博,与国家纳米科学中心的王琛、杨延莲、方巧君团队等几代科研人打磨多年,不仅发明了蛋白质对基底的吸附技术、分子伴侣的固定技术、扫描探针的脉冲技术等一系列专利技术,还对整个“拍照”的流程进行优化和摸索。
“整套(拍照)技术非常复杂,很难形成照搬流程,只能像是匠人之间的口口相传,需要知识、经验和揣摩,专业人员可能需要一年或者几年的训练时间跟着走下来,才能系统掌握。”王晨轩说。

俗话说,“台上一分钟,台下十年功”。首张“药物击靶”显微镜照不仅凝结了几代人对这一领域的积累,而且是一个集结了生物、物理、成像等多学科人才的团队多年创新的呈现。
临床价值逐渐显现:药物合成或指数级简化
看到了药物分子会“玩乐高”,对现实有什么意义吗?
答:能简化药物合成路径。“药物设计是个‘配钥匙’的过程。人们已知一个疾病相关的蛋白质结构,想设计一种反向性的药物,需要有机化学家、计算机辅助药物设计的理论化学家等一起构筑一个和蛋白质活性中心匹配的足够大的钥匙才能工作。”王晨轩对科技日报解释,药物合成越长越难,每个基团像“粘胳膊”一样,到了产业化的时候对工艺的要求更是指数级的增加。如果药物其实只需要合成原来的很小一段,1/4或者是1/8,那么难度将大大降低。
在生产一头,药物合成指数级简化;在进入身体里发挥功效时,也会事半功倍。
“小分子到体内,能够穿过一些大分子过不去的屏障。”王晨轩介绍,比如一个抗肿瘤的药物,要进入实体瘤是很困难的。因为实体瘤内部高度液化,压强非常大,大分子根本无法抵达,但小分子就不一样了,能够自由扩散,直接到达作用位点,组装后再起作用,将起到更好的疗效。
“我们清楚地在显微镜中观察到药物分子的4种寡聚态,这提示我们药物设计时应考量药物团簇是发挥作用的基本单元。”王晨轩说,所以药物设计应该把分子之间的作用考虑进去。
具体到实际工作中,王晨轩认为还有很多理论需要完善。例如,进一步地研究可以对老药物进行排查,根据以往的药物数据,来证明它和蛋白质相互作用的方法,是以哪种有序结构存在的。
“我们同时需要明确药物分子结合所需的能量,就可以通过能量来控制分子是以二聚态形式还是其它寡聚态形式存在了。”王晨轩说,其中还涉及到很多物理化学领域的理论予以支持。
要大大简化现有的药物设计程序还有很长的路要走。王晨轩说,这张显微镜照片证明了这个路径的可行性。团队的研究提供了一个工具、一套理论的基础,但具体如何实现,如何在此基础上理论联系实际,真正运用到临床药物的研发中,还需要很多工作的开展。
建筑学有LESS IS MORE(少即是多、简单就是美)的理念。首张“药物击靶”显微镜照告诉我们,这个理念对于药物设计或许同样适用。
【注】该研究工作得到中国医学科学院医学与健康科技创新工程、国家自然科学基金、医学分子生物学国家重点实验室自主研究课题、中央高校基本科研专项资金等项目的资助。
来源:科技日报 文中图片均由作者提供
编辑:岳靓
审核:朱丽
终审:冷文生
科技日报记者 张佳星
